
Se denomina vapor a una sustancia en la fase de gas que se encuentra a una temperatura más baja que el punto crítico. Debido a esta característica, el vapor se puede condensar en un líquido o un sólido incrementando su presión sin reducir la temperatura.
Es decir, es un gas que se puede condensar a temperatura constante aumentando la presión. Por otro lado, para convertir un gas no vaporoso a líquido, no es suficiente en aumentar la presión, sino que habrá que disminuir la temperatura.
Por ejemplo, el agua tiene una temperatura crítica de 374°C (647 kelvin), la cual es la temperatura más alta en la que puede existir agua líquida.
El vapor puede coexistir con un líquido o sólido. En este caso, las dos fases estarán en equilibrio, y la presión de gas será igual al equilibrio presión de vapor del líquido (o sólido).
Normalmente, la palabra vapor, si no se especifica de qué sustancia se trata, suele referirse al vapor de agua.
Definición: ¿Qué es el vapor de agua?
El vapor de agua es un gas que se produce por ebullición cuando el agua se calienta a 100°C (punto de ebullición del agua) y una atmósfera de presión.
En este punto se dice que el agua está en un cambio de fase. En este instante si seguimos suministrando calor no aumenta la temperatura hasta que se haya evaporado el agua.
En estas condiciones de presión, por encima de los 100 grados Celsius el agua pura se encuentra en estado gas.
A menudo utilizamos este término para referir nos al vapor húmedo, el aerosol de las gotas de agua que se forman al condensarse, a la niebla, etc. Sin embargo, el vapor seco es invisible.
La humedad relativa es la relación entre la presión parcial del vapor de agua en un gas (principalmente en el aire) y la presión de equilibrio del vapor saturado a una temperatura dada.
La humedad absoluta es la cantidad de vapor de agua que contiene 1 metro cúbico de aire a una temperatura determinada.
Estado de vapor
El estado de vapor es el estado en que se encuentra un gas cuando se encuentra por debajo de la temperatura crítica.
En el estado gas las moléculas que la forman no reaccionan entre sí formando enlaces moleculares, sino que tienden a repelerse mutuamente. Al repelerse, las moléculas de agua adoptan la forma y el volumen del recipiente que las contiene y tienden a separarse y ocupar todo el volumen disponible.
Características del vapor de agua
El vapor de agua es la fase gaseosa del agua y presenta una serie de propiedades físicas y químicas que lo hacen fundamental para múltiples procesos naturales e industriales.
1. Incoloro e inodoro
El vapor de agua en su estado puro es un gas incoloro e inodoro. Sin embargo, cuando se encuentra en grandes cantidades y comienza a condensarse, puede volverse visible en forma de niebla o nubes de pequeñas gotas de agua suspendidas en el aire.
2. Parte del ciclo hidrológico
Es un componente esencial del ciclo del agua. Se produce mediante la evaporación y la transpiración, asciende a la atmósfera, se condensa en forma de nubes y finalmente regresa a la superficie terrestre en forma de precipitación (lluvia, nieve o granizo).
3. Gas de efecto invernadero
El vapor de agua actúa como un gas de efecto invernadero, absorbiendo y reteniendo el calor en la atmósfera terrestre. Regula la temperatura del planeta y desempeña un papel clave en la climatología y la meteorología.
4. Expansión y presión
Cuando el agua se convierte en vapor, experimenta una gran expansión de volumen. A alta temperatura y presión, este fenómeno es aprovechado en motores y turbinas para generar movimiento y energía mecánica.
5. Conductividad térmica y capacidad calorífica
El vapor de agua tiene una alta capacidad calorífica, lo que significa que puede almacenar y transferir grandes cantidades de calor. Por ello, se usa en sistemas de calefacción, producción de energía y procesos industriales donde se requiere transmisión de calor.
6. Cambios de estado y condensación
Al enfriarse, el vapor de agua se condensa en pequeñas gotas de líquido, formando nubes, niebla o rocío. Este proceso es clave en la formación de precipitaciones y en la regulación del equilibrio térmico de la atmósfera.
Diferencia hay entre gas y vapor
El vapor es un tipo de gas, pero no todos los gases son vapor.
Si comprimimos un gas manteniendo la temperatura, el gas no cambia de estado, sigue siendo gas. En cambio, al aumentar la presión a temperatura constante, al vapor sí que puede volverse líquido.
El gas ocupa totdos el espacio disponible mientras que el vapor no se comporta de esta forma.
Importancia del vapor
El vapor es un elemento esencial para la vida en la Tierra, desempeñando un papel fundamental en diversos procesos naturales y tecnológicos.
Su presencia en la atmósfera influye en el clima y en el ciclo hidrológico, mientras que su aprovechamiento por parte del ser humano ha sido clave para el desarrollo de la industria y la producción de energía. Desde la Revolución Industrial hasta la actualidad, el uso del vapor ha impulsado avances significativos en la generación de trabajo mecánico y electricidad.
Importancia en el medio ambiente
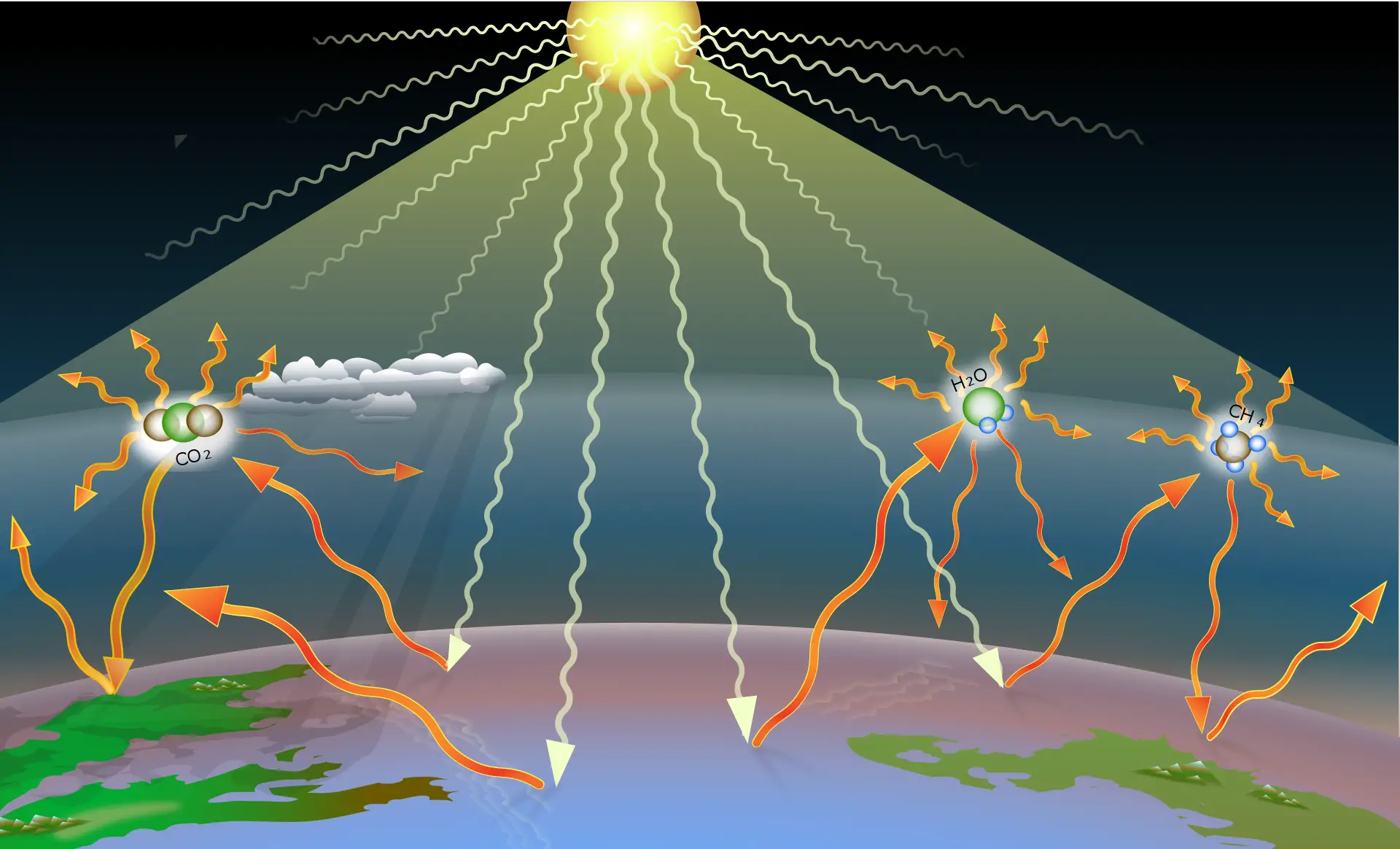 El vapor de agua es un componente crucial de la atmósfera terrestre y un gas de efecto invernadero que, al igual que el dióxido de carbono, contribuye a la regulación térmica del planeta. Absorbe y retiene parte de la radiación solar reflejada por la superficie terrestre, ayudando a mantener una temperatura adecuada para la vida. Sin embargo, cambios en su concentración pueden influir en el calentamiento global y en la variabilidad climática.
El vapor de agua es un componente crucial de la atmósfera terrestre y un gas de efecto invernadero que, al igual que el dióxido de carbono, contribuye a la regulación térmica del planeta. Absorbe y retiene parte de la radiación solar reflejada por la superficie terrestre, ayudando a mantener una temperatura adecuada para la vida. Sin embargo, cambios en su concentración pueden influir en el calentamiento global y en la variabilidad climática.
Además, el vapor de agua desempeña un papel esencial en el ciclo hidrológico, que es el proceso continuo de circulación del agua en la Tierra. A través de la evaporación, el agua pasa de ríos, océanos y lagos a la atmósfera, formando nubes que posteriormente producen precipitaciones.
Este ciclo es vital para el mantenimiento de los ecosistemas, la regulación climática y el suministro de agua dulce para el consumo humano, la agricultura y otras actividades esenciales.
Importancia en la industria
Las propiedades del vapor permitieron el desarrollo de la máquina de vapor, un invento que transformó por completo la industria y la sociedad durante la Revolución Industrial.
Gracias a la capacidad del vapor para generar movimiento, se implementaron motores de vapor en fábricas, facilitando la mecanización de la producción y aumentando la eficiencia de los procesos industriales. Esto marcó el inicio de una era de modernización, con avances en sectores como la minería, la manufactura y el transporte.
En el ámbito del transporte, las locomotoras de vapor revolucionaron la movilidad terrestre, permitiendo viajes más rápidos y eficientes. Del mismo modo, los barcos de vapor facilitaron la expansión del comercio marítimo, reduciendo los tiempos de navegación y aumentando la capacidad de carga.
Estos avances contribuyeron a la integración de mercados y al crecimiento económico a nivel mundial.
Generación de electricidad
El vapor sigue desempeñando un papel crucial en la producción de electricidad, especialmente en las centrales térmicas y nucleares.
En estas instalaciones, se utiliza la energía térmica obtenida de combustibles fósiles (como carbón, gas y petróleo) o de la fisión nuclear para calentar agua y generar vapor a alta presión. Este vapor impulsa turbinas de vapor conectadas a generadores eléctricos, transformando la energía térmica en energía mecánica y, posteriormente, en electricidad.
Este principio de funcionamiento es la base de muchas plantas de generación de energía en todo el mundo, ya que el vapor permite aprovechar diferentes fuentes de calor para producir electricidad de manera eficiente.
Además, las turbinas de vapor han evolucionado con mejoras tecnológicas que aumentan su eficiencia y reducen el impacto ambiental, contribuyendo a la transición hacia un sistema energético más sostenible.